癌組織由来の血中遊離DNAの存在
| Dennis Loらのグループが、妊婦の血液中に胎児由来の遊離DNAが存在することを発見したのは、1997年のことであるが、血液中の癌DNA存在の発見はかなり古く、1948年が最初の発見と思われる。これまでの研究により、担癌患者は健常人と比べて、総じて血中遊離DNAの濃度が高いことがわかっている。しかしながら、担癌患者の血中遊離DNAの濃度は健常人のレベルであることもあるため、血中遊離DNAの濃度を癌の診断に利用するのは難しい。癌組織由来の血中遊離DNAの存在は、妊婦血中への胎児DNAの漏出と同じく、癌細胞がアポトーシスにより壊れる際に分解したDNAが血液中に漏れ出ることによる。病状が進行した担癌患者の場合、血中癌DNAの割合は血中全DNAに対して1%~50%であることが報告されている。 母体血液中の胎児由来DNA分析を診断に結び付けることは比較的容易であるが、癌の場合には、癌の原因も様々であり、癌変異も多様であることから、実用的な診断を実現することは容易でなかった。このような背景の中、血中の癌DNAをNGSによりゲノムワイドに解析できれば、癌診断や癌治療に役立つと期待されており、2010年頃から研究成果が発表されている。 |
血中癌DNAの全ゲノムシーケンシング解析
| 癌組織由来の血中遊離DNAをNGSにより解析し、癌特異的変異を同定できることを示した成果を昨年末に2つのグループが発表している。Johns Hopkins Kimmel Cancer CenterのLearyらは、7人の大腸癌患者と3人の乳癌患者、ならびに10人の健常人から血中遊離DNAを調製した後、Illumina シーケンサーにより50 bpのペアエンド・リードで癌DNAを含む全ゲノムシーケンシングを行った。配列決定量はハプロイドゲノムに対して10倍前後(冗長度が10程度)であったので、コピー数変異(CNV)、リアレンジメント、大きな欠失および染色体構造異常など、大きな構造変化は検出できているが、一塩基置換のような小さな変異は検出されていない。
一方、妊婦血中における胎児DNAの存在を発見したLoのグループは、4人の肝細胞癌(Hepatocellular Carcinoma;HCC)患者と16人の健常人から血中遊離DNAを調製し、Illumina シーケンサーに50 bpまたは75 bpのペアエンド・リードで癌DNAの全ゲノムシーケンシング解析を行ったことを発表した。Loらのグループの配列決定量は、ハプロイドゲノムに対して冗長度が約30であったので、CNVなどの大きな構造変化だけでなく、一塩基変異(Single Nucleotide Variation;SNV)を検出できることを証明した。シーケンシングエラーが気になるが、健常人の血中遊離DNAの全ゲノムシーケンシングの結果と比較することにより、エラー率を算出した。その結果、検出された変異候補については、エラー率が0.38%と低く、検出された変異の多くは癌に特異的であることがわかった。4人のHCC患者の血中癌DNAの割合は血中全DNAに対して2~53%であった。血中癌DNAの割合が53%の場合には、癌組織のNGS解析で検出されたSNVのうち、約94%を検出できる。一方、その割合が2%の場合には、癌DNAのリード数が少なくなるために、癌特異的SNVの検出率は約15%になることを明らかにしている。
以上の研究成果を総合すると、血中癌DNAの全ゲノムシーケンシング解析により、癌特異的なゲノムの構造異常やSNVを検出できるものの、患者により血中癌DNAの割合のばらつきも大きいために、網羅的に癌特異的変異を検出することは容易でない。さらに、実用上利用できる診断結果を得るには、シーケンシング量も冗長度30程度では不十分で冗長度100以上のNGS解析を行う必要があり、コスト面でも解決すべき課題がある。
|
TAm-Seq:癌ゲノムのターゲットシーケンシング
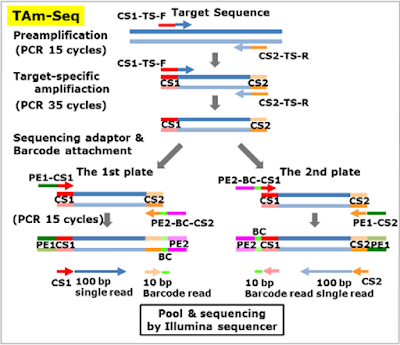
| 癌ゲノムのNGSターゲットシーケンシングについては、Cancer Research UK Cmabrige Research Institute のForshewら が開発したTAm-Seq法(下図参照)が優れているので、紹介したい。 まず、既存の癌関連変異が報告されている癌関連遺伝子の特定部分(Target Sequence;長さ150~200 bp)をPCRで増幅するためのプライマー(CS1-TS-FとCS2-TS-R)を調製する。Forshewらの論文では、PIK3CA遺伝子2ヶ所、EGFR遺伝子12ヶ所、BRAF遺伝子1ヶ所、PTEN遺伝子16ヶ所、KRAS遺伝子1ヶ所、TP53遺伝子16ヶ所の合計48ヶ所の癌関連遺伝子の特定部分をターゲットとしている。合計の長さは5,995 bpである。なお、PCRプライマーには、Illuminaシーケンサーにより配列決定を行うためのユニバーサルプライマー配列CS1とCS2が付加されている。1対のプライマーを用いて15サイクルのPCRによりターゲット配列のプレ増幅(Preamplification)を行う。続いて、同じプライマーを用いて35サイクルのPCRによりターゲット配列を特異的に増幅する。 次に、この断片をもとに、フォワード方向とリバース方向にそれぞれ100 bpのリード長でIlluminaシーケンサーにより配列決定を行うために、タグ(PE1とPE2)を付加する。上図に示すように、フォワード方向とリバース方向にシーケンシングするためのタグ付加は別々に行う。増幅したターゲット配列は48種類あるので、これらを混合し、共通のプライマーセット(PE1-CS1とPE2-BC-CS2もしくはPE2-BC-CS1とPE1-CS2)を用いた15サイクルのPCRにより、シーケンシング用のアダプターとサンプル識別用バーコードを付加する。バーコードは10 bpの配列からなり、複数の患者由来のサンプルをまとめてシーケンシングする際に、サンプルの由来を識別するために付加している。 このようにして調製したシーケンシング用サンプルを用いて、100 bpのリードと10 bpのバーコード配列を決定することにより、各患者由来の癌関連遺伝子の特定部分を深く解読することができる。冗長度は、血中遊離DNA中の癌DNAの存在割合に応じて変えるが、Forshewらの論文では、目的別に3,250倍、5,600倍、650倍の3通りの冗長度でシーケンシングを行っている。癌DNAの存在割合が2%以上あれば、冗長度650(以上)のシーケンシングが適していることが示されている。 上述の全ゲノムシーケンシングでは実用的な変異同定は行えなかったが、このTAm-Seqでは、目的変異の出現回数が10以上になる結果が得られており、同定精度の面で実用的な診断が可能であるといえよう。また、PCRで増幅するターゲット領域はプライマー配列を変えることにより自由に設計できるので、多様な癌変異を一度に解析できる点でも利点がある。同定精度はDigital PCR法と同等であることが示されており、かなり精度が高い。なお、Digital PCRの場合には、特定の癌変異しか適用できないし、TP53遺伝子のように、遺伝子内に多様な変異が観察される場合には適用できないという欠点がある。 |
癌ゲノム・エキソームシーケンシングによる血中癌DNAの解析
| 上述のターゲットシーケンシング(TAm-Seq法)は優れた方法であるが、解析ターゲットが限定される点が難点である。これに対して、エキソームシーケンシングは、遺伝子やたんぱく質の機能に影響を及ぼす可能性がある領域を網羅的に解析できることが利点がある。Cancer Research UK Cambridge Institute/Cambridge大学のNitzan Rosenfeldのグループは、血中癌DNAのエキソームシーケンシングにより、癌変異を高精度に同定できる上、化学療法によって生じた薬剤耐性の原因変異を治療の経過を追って解析できることを明らかにした。 化学療法を施した6人の進行癌患者(2人の乳癌患者、3人の卵巣癌患者、1人の非小細胞性肺癌患者)について、約2 mlの血液から調製した血中遊離DNAをもとに、エキソームシーケンシング、TAm-Seq法(上述)およびDigital PCR法を用いて、化学療法の経過に伴う癌変異の出現変化を分析した。エキソームシーケンシング(冗長度=31~160倍)については、化学療法直前に調製したエキソームのシーケンシングに加えて、化学療法後2年以内に1~4回エキソームシーケンシングを行った。 一部の患者については、バイオプシーにより採取した癌組織のDNAをもとにエキソームシーケンシング解析を行い、CNV(Copy Number Variation)と変異を検出した。得られた結果を血中遊離DNAをもとに得られた変異同定結果と比較したところ、変異出現頻度について両者の間で高い相関が認められた。また、血中遊離DNAからは、バイオプシーにより採取した癌組織からは検出できなかった変異を多数検出できることがわかった。この理由としては、バイオプシーでは限られた癌組織からしか変異を同定できない上、化学療法後にバイオプシーを行うことは困難であることから、癌組織のシーケンシングでは化学療法後に生じた変異を検出できないことが挙げられる。 化学療法後のエキソームシーケンシングでは、各患者において化学療法後に薬剤耐性の原因となる変異の出現頻度の上昇が観察された。たとえば、乳癌患者にpaclitaxelを投与した後では、paclitaxelへの耐性の原因となることが知られている「PIK3CA遺伝子の変異」の割合が上昇した。別の乳癌患者にtamoxifenとtrastuzumabに投与したところ、tamoxifen耐性と関係する「 MED1遺伝子の変異」の割合が上昇した。さらに、この患者にlapatinibとcapecitabineを投与したところ、lapatinibの耐性と関係する「GAS6の変異」が増えることも判明した。また、卵巣癌患者にcisplatinを投与したところ、cisplatin耐性と関係していることが報告されている「癌抑制遺伝子RB1の変異」の頻度が上昇した。他方、非小細胞性肺癌患者に対してgefitinibを投与したが、投与開始時には全く検出されなかった「EGFR変異(T790M)」が109日後には13%の頻度で検出された。なお、このEGFR変異はgefitinibへの耐性と関係することが報告されている。 以上のように、血中癌DNAのエキソームシーケンシングは、癌変異を網羅的に検出できる上、検出精度もTAm-Seq法やDigital PCR法とも遜色がないことが示された。また、血中癌DNAの解析は癌組織のバイオプシーとは異なり、少量の血液を非侵襲的に採集するだけなので、患者への負担が少ない。さらに、癌手術後や化学療法後は癌組織を採取することは困難であるので、血中癌DNAのエキソームシーケンシングは癌の治療経過をフォローする上で有効である。 |